傳統風險評估在處理個體差異時,通常依賴預設的不確定係數(uncertainty factors, UFs)。本研究旨在推動次世代風險評估(NGRA)中體外新穎性方法學(NAMs)模型的應用,驗證是否可透過實驗數據直接估算「化學物質特異性的人體個體差異」,以提供更具保護力且精確的風險評估依據。
本研究採用131株來自歐洲與非洲族群的人類淋巴母細胞(LCLs),測試53種涵蓋工業化學品、藥物與農藥等不同性質的化學物質,並結合貝葉斯建模(Bayesian modeling)分析濃度–反應關係,計算每株細胞的毒性起始點(point of departure, PoD)。最終針對18種具有明顯細胞毒性的化學物,進一步計算其毒效動力學變異因子(TDVF₀₅)。
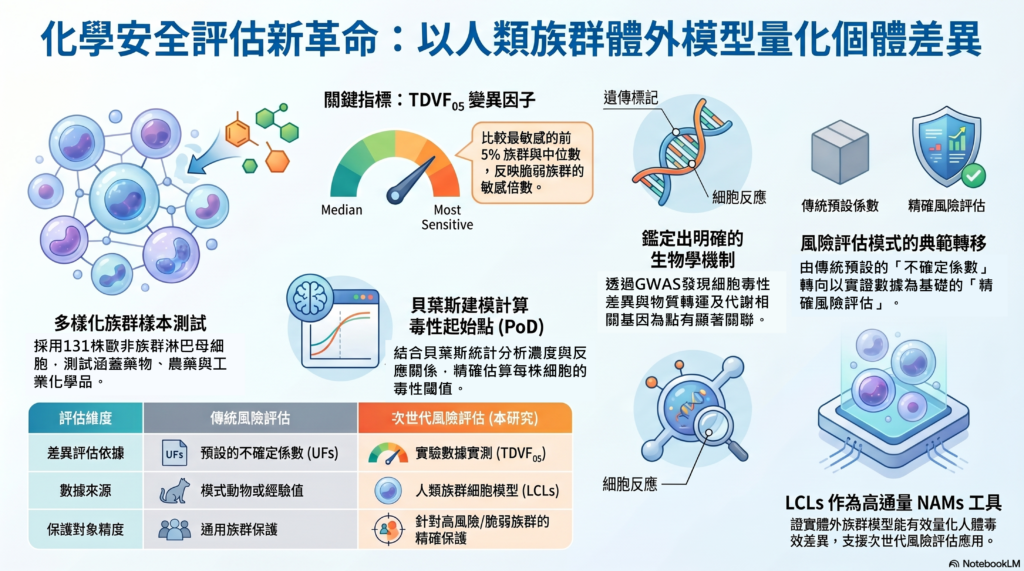
所謂TDVF₀₅,是將所有細胞的PoD依毒性敏感程度排序,選出最敏感的前5%族群,與整體族群的中位數相比,計算兩者之間的差異倍數。簡言之,此指標反映「最脆弱族群相較於一般人,其對化學物質的敏感程度高出多少倍」。透過此類數據,可使風險評估由傳統預設係數轉向以實證為基礎,進一步提升對高風險族群的保護能力。
此外,透過全基因體關聯分析(genome-wide association study, GWAS),研究鑑定出多個與細胞毒性變異相關的基因位點,主要涉及物質轉運與代謝相關基因,顯示個體間對同一化學物質的敏感差異具有明確的生物學機制基礎。整體而言,本研究顯示LCLs模型為一種可行的高通量NAMs工具,可用於量化人體毒效差異並支援NGRA應用。然而,體外細胞模型在涵蓋體內複雜不良效應方面仍具限制,未來應用時亦需審慎考量與體內劑量動力學之對接與整合。
編譯:何瑀琪 博士
校稿:林嬪嬪 研究員

